From PGI
Contents
사람과 개의 마지막 사슬
그림 1 진돗개
2012년 5월 한 번 주인을 섬기면 충성을 다하는 진돗개에 대한 염기서열이 처음으로 해독되어 우리나라 고유의 품종으로 확인되었다. 그와 함께 사람과 360가지 이상의 유전적 소양이 비슷하여, 인간의 질병 연구에 있어서 하나의 모델적인 연구로도 활용될 것으로 확인되었다.
인간과의 생리학적 유사성이 높고 인수 공통 전염병이 많다는 점 등 때문에 개를 연구 대상으로 선택하는 학자들이 많다. 개는 다양한 유전적 난치 질병 치료법 연구에 활용될 뿐 더러 향후 사람의 질병모델 동물도 생산할 수 있고, 신약 및 세포치료제 개발에 응용할 수 있을 것이다.2005년 황우석 박사는 개를 복제하면서 350년 간의 수의학 의약품과 약물들은 병의 진단과 치료를 위한 동물의 발달을 언급하였다. 이처럼 인간과 동반자 역할을 하는 개와 같은 동물의 질병에 대한 연구는 끊임없이 지속되고 있다. 개의 유전체는 이미 완성되었으며, 인간 유전체 지도와 비교하며 개과의 동물 유전학이 발달하여 미래에 대한 기대를 높이고 있다.
인간과 개의 유전체학
그림 2 개의 다양한 품종
인간게놈프로젝트는 2명의 인간 유전체 서열의 독립적인 초안 버전과 약 3만개의 유전자를 99% 식별하여 2004년 공식적인 완료를 선언하였다. 이와 늑대(Canis lupus)류의 DNA를 비교하여 생어시퀀싱(1.5x)으로 2번, NGS(7.8x)를 이용하여 1번 분석하였다. 푸들(poodle)과 복서(boxer)의 유전체에서 copy number 변이, 전사체를 매핑하여 염색체 구조를 이해하고 누락된 유전자를 찾았다.
개 유전체의 이용은 인간의 복잡하고 어려운 유전 질환의 이해를 위해 20년 이상 이루어져왔다. 이번 연구는 회색 늑대(Canis lupus)가 최소 3만년 전 국내에 들어오고, 독립적인 그룹과 번식의 발달으로 다양한 종으로 분화된 것에서 시작하여,인간과 개의 건강에 대한 관심 유전자를 식별하기 위한 자료를 제공하였다.
[그림 2]에서 보다시피, 개의 많은 품종은 빅토리아 시대 동안 개발되어 몇 백 년에 걸쳐 진화되어 왔다. 대부분의 품종이 빅토리아 시대의 인기 있던 종들의 후손으로 물리적 특성에 대한 선택성이 발휘된 사육 프로그램에 의해 진화되었다. 그 중에는 열성 질환을 보유한 순종도 있을 것이며, 이러한 종들은 특정 장애에 대한 위험이 높다.
개과의 유전력
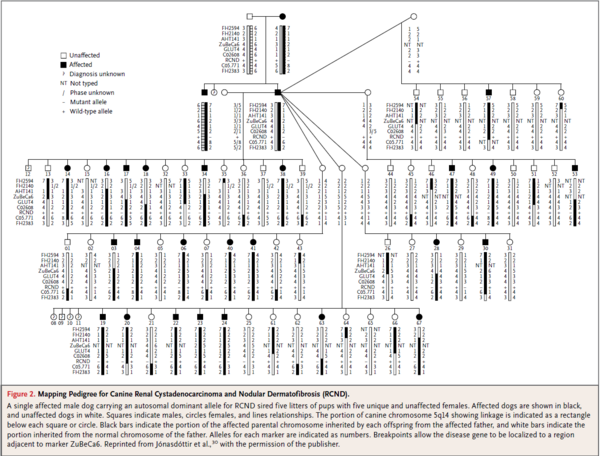
그림 3 RCND에 의한 개 유전자 매핑
[그림 3]은 독일산 셰퍼드의 유전적 신장 낭종암과 피부 결절 종양(RCND; renal cystadenocarcinoma, nodular dermatofibrosis)에 의한 개의 유전자를 매핑한 것이다. RCND는 인간의 Birt–Hogg–Dubé syndrome(BHD)와 유사한 신장과 피부의 유전 장애로, 선천성 암 증후군 중 하나이다. 종양이 신장과 피부 등 고밀도의 콜라겐 기반인 결절 부위에서 나타난다. 질병의 대립 유전자는 높은 침투성과 상염색체 우성 유전으로 10,000분의 1의 확률로 유전된다. BHD는 개의 5q12에 위치하는 데, 인간에서는 17p12q11에 위치하는 등 유사하다. BHD는 종양억제 단백질인 폴리큘린(folliculin; 발정호르몬) 변이를 가지고 있어서, AMP-활성화 단백질 키나아제와 라파마이신(rapamycin; 면역억제제, 노화억제제) 감지 신호 경로에 영향을 끼친다.
개와 인간의 유사한 유전 변이를 확인하는 세 가지 중요점이 있다.
첫 번째는, 단일 형통의 큰 개는 지노타이핑(genotyping)을 통해 인간에 대한 자료 수집이 많이 필요하다. 두 번째는, BHD는 동일한 유전 배경을 가진 품종의 질병 발현에 상당한 변이에 연관성이 있으므로 유사 장애와의 구별이 어렵다. 세 번째는, 인간의 변이 이전에 개의 변이가 확인되었다. 기면증(narcolepsy), 구리 중독증, 배튼씨병(neuronal ceroid lipofuscinosis), 어린선(ichthyosis; 피부가 건조하여 물고기 비늘처럼 되는 유전성 각화증) 등이 이에 해당한다.
예를 들어, 도베르만(Doberman pinscher)의 기면증 같은 경우, 신체 감각 조절에 도움을 주는 수면발작 관련 뇌단백질인 히포크레틴(hypocretin) 수용체 돌연변이를 식별해야 하는데, 분자생물학적 수면 인식 경로는 개의 변이가 먼저 확인되었다. 또 테리어(American Staffordshire terriers)의 배튼 씨 병(neuronal ceroid lipofuscinosis, Kuf병)은 인간에서는 성인이 되서야 발병하는 유전장애이다. 배튼 씨 병은 arylsulfatase G(ARSG) 유전자가 엑손 2번의 R99H 돌연변이로 인해, sulfatase 활동이 75%로 감소된다. 개의 질병 변이를 먼저 확인하였기 때문에 인간에서 발생하는 배튼 씨 병의 새로운 유전자를 식별하고, sulfatase 결핍과 질병경로에 대한 정보를 제공 받을 수 있다는 이점이 있다.
개의 품종 구조
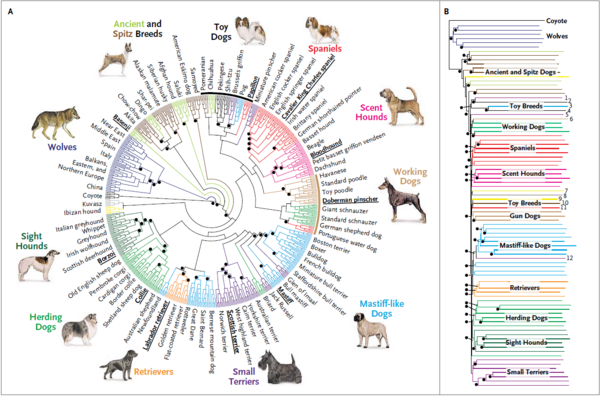
그림 4 개의 품종 구별 지도
[그림 4]는 유럽의 400개 이상 품종과 미국의 독립적 진화를 거친 173개 품종을 나타낸 것으로, 개의 질병 유전자 매핑에서 반복되는 서열을 이용하여 품종을 구별한 지도이다. 핀란드나 아이슬란드 등의 지리적으로 고립된 나라에서 인간을 연구하여 개와의 이질성을 줄여 나타내었다.
예를 들어, 복잡한 질병 유전자와 해로운 대립유전자에 대해 알아보기 위해, 유전성 유방암 환자인 아이슬란드 여성의 999del5 BRCA2 돌연변이를 발견했다. 임상 표현형과 이질성이 높은 간질은 영국의 작은 와이어헤어 종의 5%, 전체 개의 25%가 간질 돌연변이인 EPM2B를 가진다. 라고토 로마그놀(Lagotto Romagnolo)의 번식에서 간질 유전자 LGI2를 발견하였으며, 이것은 인간의 간질 유전자 LGI1에서 상동체의 변형에 의해 나타난 것이다. 닥스훈트(dachshunds)는 10대에서 발병하는 간질의 심각한 형태인 Lafora 질환의 가능성이 있다. Lafora 질환은 신경세포에 신경 증상이 없는 노령견에서 발견되며, 거리감각불능, 거리감각 과대 및 과소, 떨림, 오한, 경련, 무기력, 발작, 간질, 절뚝거림, 넘어짐 등의 증상을 보인다. 주로 인간에서 나타나는 근경련 질병을 연상시키는데, 900대 1의 비율에 의해 유전자 발현에 변이가 생겨서, 해로운 EPM2B(간질 발현 단백질)에 반복적인 서열의 확대로 인해 발병한다. 이처럼 간질과 같은 복잡한 질병을 연구하기 위해, [그림 4]와 같이 다양한 다른 품종의 장애를 연구하는 것이다.
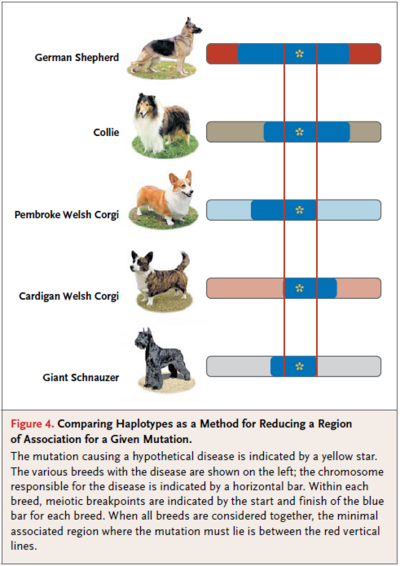
그림 5 품종 별 유전체 구조의 관련성에 따른 식별
품종 별 유전체 구조가 유전자 매핑에 이점을 제공한다. 유전자에 연결된 마커에 의해 매핑이 빠르게 되며, 개와 인간 사이의 SNP가 적어 초기 매핑에 식별이 용이하다. [그림 5]는 품종 별 관련성에 따라 교배가 용이하며, 염색체의 관심지역이 단상형으로 유전자형이 하나인 상황을 보여준다. 단상형인 유전자가 부재인 부위를 공유하는 DNA 조각을 식별하면, 같은 장애와 관련된 품종을 비교할 수 있다.
2006년 Goldstein과 동료들은 개의 망막위축증과 유사한 인간의 망막색소변성증(retinitis pigmentosa)을 확인하였다. 푸들을 비롯한 수십 가지 품종에서 장애가 나타났으며, 추가적으로 SNP 분석을 실시하여 14개의 품종에 영향을 끼치는 106개 단상형 새로운 돌연변이를 차세대 시퀀싱(NGS; next generation sequencing)으로 확인하였다. 이를 통해 형태학적 기능에 대한 품종간의 관계에는 동일 돌연변이를 공유할 수 있다는 점이 밝혀졌다.
개의 형태학적 분석
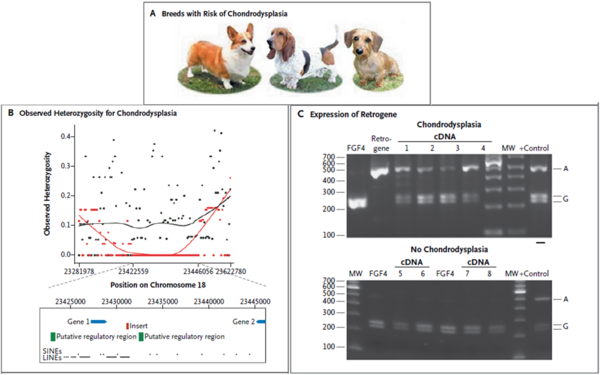
그림 6 짧은 다리를 가진 20가지 이상 품종에 대한 특징
[그림 6]는 형태학적 분석으로개와 사람의 관련 질환 및 후보 유전자를 확인하기 위해, 짧은 다리를 가진 20가지 이상의 품종에 대한 특징을 나타낸 것이다. 닥스훈트, 코기(corgi), 바셋하운드(basset hound)를 포함하여 짧은 다리를 가진 20가지 이상의 품종들은 연골 형성 이상증(chondrodysplasia)을 가지고 있다.
이에 연골 형성 이상증을 가진 95가지 품종의 염색체 18번을 GWAS(Genome wide association study) 분석하였다. 공통적인 특징을 공유하는 품종과 전혀 관련이 없는 품종을 비교하여,fgf4 retrogene의 발현에 차이가 발생하는 것을 확인하였다. 섬유아세포의 성장인자가 암호화되고, 인트론의 신호가 누락되는 등의 특징이 나타나며, 이는 뼈가 길게 성장하는 부위가 조기 폐쇄되는 것의 원인이 된다. 뼈가 길게 성장하지 못한 이유는 발현시기를 놓치거나, RNA 발현수준이 낮거나, retrogene의 잘못된 지역화(mislocalization)이다.
또한 인간의 질병에 유사하여 중요한 부위로 확인되며, 형태학적으로 몸의 크기, 다리의 폭, 털 색상은 조절하는 loci를 확인하였다. 질병 대립 유전자는 개의 특정 모양을 선택하는 결과를 나타내었는데, 로디지아 리지백(Rhodesian ridgeback) 종은 머리에서 꼬리까지의 능선과 피부양동(dermoid sinus), 번식에 관련된 신경관의 결함 등에 나타났다.
2005년 Lindblad-Toh와 동료들의 연구에서는 100마리의 20가지 케이스의 열성 형질에 관련된 다섯 가지 유전자와 5만 개 이상의 SNP를 확인하였다. 또한 Wilbe과 동료들의 연구에서는 스코티아 덕 톨링 레트리버(Nova Scotia duck-tolling retrievers) 종에서 루푸스(SLE; systemic lupus erythematosus)에 대한 유전자를 식별하였다. 레트리버는 SLE 등의 자가면역질환이 많이 발병하며, 디스템퍼 바이러스(canine distemper virus) 2가지 종에 감염되어도 생존하는 등의 특징이 있다. 이는 22,000개 SNP에 따른 강한 면역 시스템을 보유하고 있기 때문에, 5가지 loci에서 PPP3CA, BANK1, DAPPI 등 T세포 활성화 관련 유전자가 발현된다.
개의 번식과 암의 유전자 치료
개와 인간에서 질병에 관련된 사망의 가장 흔한 원인인 암은 개뿐 만이 아니라, 인간의 건강에 큰 영향을 끼칠 가능성이 있다. 개에서 치명적인 수지상세포 종양이나 조직구 육종(sarcomas) 등의 희귀 종양은 연구 모델로서의 개의 역할을 나타낸다.
그림 7 버너스 마운틴 개(Bernese mountain dogs)
개에 나타나는 희귀 종양의 두 가지 형태는 다음과 같다. 피부와 기저 종양은 다리에서 발병하여 림프절과 혈관에 전이되는 변이 형태로 비장, 간, 폐에 영향을 미치는 파종성(다른 질환과 관계된) 시스템이다. 조직구 육종은 버너스 마운틴 개(Bernese mountain dogs)에서 주로 발병하며 그 중 약 20%는 치명적인 영향을 끼치기도 한다. 인간의 랑게르한스 섬 세포의 조직구와 유사한 장애라서 임상적 원인 파악에 중요하다.
조직구 육종 분석을 위해 프랑스, 미국, 네덜란드의 버너스 마운틴 개를 GWAS 분석을 수행하였다. 18번 염색체에서 두 개의 loci에 걸쳐 MTAP 유전자와 INK4A-ARF-INK4B 발현 단백질의 변이를 확인하였다. 하나 이상의 변이를 포함하는 단상형 유전체의 40%가 질병에 동형접합성이지만, 나머지 60%는 결국 암으로 사망한다.
개의 염색체 11번은 인간의 염색체 9p21에 해당하며, 암과 연결된 부위이다. 여러 가지 암이 MTAP-CDKN2A 유전자 지역에서 변이가 생겨 발병하며, 버너스 마운틴 개는 이러한 암 발병의 변이 연구를 위한 생물학적 모델로 이용된다.
2001년 Acland와 동료들의 연구에서는 간장의 선천성 흑내장(amaurosis) 유형2인 망막의 위축 형태를 연구하였다. 이는 인간에서도 발병하는 것으로, 주로 출산 후 실명의 원인이 되는 RPE65 유전자 돌연변이에 의한 것이다. 개와 인간은 RPE65 변이가 동형접합성이며, 재조합한 아데노 바이러스(adeno virus)를 이용하여 망막 위축성 장애에 대한 모델을 제안하였고, 100가지 이상의 품종에서 발생하는 장애를 치료하기 위해 개의 망막 질환에 관련된 18개 유전자를 발견하였다. 또한 불 테리어(bull terriers), 도베르만을 이용하여 개의 분리불안, 침략적 지배성격, 강박 신경증 등의 이상행동에 대해 연구하였고, 염색체 7번의 CDH2 유전자 변이에 의한 것임을 확인하였다.
맺음말
개의 건강에 대해 이해하고자 하는 것은 우리가 자신에 대해 알고 싶은 것과 같을 정도로 유사한 유전체 서열을 보유한다. 100세 시대가 되어가고 있는 지금 이 시점에서, 우리의 질병을 알기 위해서는 우리와 유사한 동물들의 정보가 중요하다. 가장 오랜 시간 사람과 함께 해온 개의 경우, 종의 다양성과 다양한 질환에 대한 반응도 비슷하다. 앞으로는 동반자 동물의 질병에 대해서도 많은 관심을 가져야 할 것이다.
참고문헌
Both Ends of the Leash — The Human Links to Good Dogs with Bad Genes
http://www.nejm.org/doi/full/10.1056/NEJMra1204453
Annotation of the domestic dog genome sequence: finding the missing genes.
http://www.ncbi.nlm.nih.gov/pubmed/22076420
Genomic analyses of modern dog breeds.
http://www.ncbi.nlm.nih.gov/pubmed/22231497
저자
글 : Park.Hyeonji
편집 : Ahn.Kung
키워드 : 늑대(Canis lupus), RCND(renal cystadenocarcinoma, nodular dermatofibrosis), Birt–Hogg–Dubé syndrome(BHD), folliculin, rapamycin, 기면증(narcolepsy), 배튼씨병(neuronal ceroid lipofuscinosis), 라고토 로마그놀(Lagotto Romagnolo), 닥스훈트(dachshunds), 망막색소변성증(retinitis pigmentosa), 코기(corgi), 바셋하운드(basset hound), 연골 형성 이상증(chondrodysplasia), 로디지아 리지백(Rhodesian ridgeback), 레트리버(Nova Scotia duck-tolling retrievers), 루푸스(SLE; systemic lupus erythematosus), 디스템퍼 바이러스(canine distemper virus), 버너스 마운틴 개(Bernese mountain dogs), 흑내장(amaurosis), 불 테리어(bull terriers) 등